1. 서 론
온실가스는 다양한 배출 경로를 통해 대기로 배출된다. 산업 활동으로 인한 인위적인 배출 외에도, 온실가스는 토양, 습지, 바이오매스 연소와 같이 자연적으로 배출되는 경로도 있다. GWP20의 개념이 최근에 주목받고 있는 데, 이는 10~20년 동안의 상태가 미래에 큰 영향을 미치는 비상상황으로 간주되는 것으로 20년을 기반으로 온실가스의 강도를 계산하는 방법이다(Pérez-Domínguez et al., 2021). 이러한 자연 배출은 인위적인 배출과 비슷하거나 그보다 많은 양일 것으로 알려져 있으며(Warneck, 1999), 특히 메탄은 GWP100에서 이산화탄소(CO2)의 23%를 차지하지만, GWP20에서는 CO2 등가교환으로 80%를 차지한다.
최근 온실가스와 관련해서 기후변화의 영향도 크다. 기후 변화로 인한 온도 상승이 수온의 변화로 이어진다는 것에 관한 다양한 연구가 진행된 바 있다(Stockle et al., 1992; Sinokrot and Stefan, 1993). 수온에는 복사열, 복사열의 차단 정도, 수계로부터 나오는 하천수 및 지하수의 온도, 수면에서의 열 교환 등 다양한 요인이 영향을 미치는 것으로 알려져 있다. An and Lee(2013)는 국내에서 2009~2011년까지 873~1,083건의 관측을 통해 수온과 기온 간의 관계를 분석하였다. 수온과 기온 간의 상관 계수는 0.9 이상으로 측정되었다. 이러한 수온 상승은 수자원 측면에서 수질에 영향을 미칠 수 있다(Kalff, 2004). 수온 상승은 낮은 층에 분포된 조류 및 미생물의 활동 증가로 이어져 산소 소비가 증가하고 용존 산소가 감소를 유발한다. 이는 층화된 호소 내에서 메탄이 발생할 수 있다. 메탄은 습지, 호소, 하천 등과 같이 수환경이 중요한 원천으로 알려져 있다(Maeck et al., 2013; Hamdan and Wickland, 2016). 수중 환경에서의 메탄발생에 대한 영향 요인을 확인하고 메탄 배출량을 측정하여 메탄발생량을 추정하는 연구가 다수 진행되어왔다. 그러나 호소에서의 메탄 배출은 다양한 환경 요소의 영향을 받기 때문에 불확실성이 크다. 이에 Liu et al.(2020)은 메콩 강의 메탄 플럭스의 공간적 가변성을 특성화기 위하여 기포 관측을 통해 메탄의 기포 확산에 의한 발생량을 정량화하였다. 기포 관측기기 위치 주변에서 채취한 퇴적물 코어를 분석하여 메탄 발생의 잠재적 생성량 및 산화속도도 함께 추정하였다. Tušer et al.(2017)도 수중 조사를 기반으로 개소로 흐름에서의 가스 기화에 대한 계절적 및 공간적 분포를 조사하였다. 그 결과 가스생성은 온도에 의해 계절적 영향이 주요 요인이며 하천수 유입으로 인한 유기 물질의 유입이 생성원인임을 확인하였다. 수심이 얕은 경우 수온의 변동성은 크고 바닥층에 수압이 상대적으로 낮기 때문에 박테리아 활동 증가 및 가스 생성을 용이하게 한다. 또한 기포가 수면으로 이동하는 시간이 짧아 기포가 충분히 용해되지 못한다(McGinnis et al., 2006). Linkhorst et al.(2020)은 브라질의 두 개의 저수지에서의 메탄 발생을 음향측심기(echo sounder)와 버블트랩(bubble trap)을 사용하여 관측하였다. 저수지의 다른 지역보다 유입부에서 평균 메탄 발생량이 2배 이상으로 관측되었고, 영양소가 풍부한 저수지에서는 4배 이상으로 관측되었다. 또한 다른 연구에서는 대기 압력에 따라 메탄 발생량의 차이가 나타날 수 있다는 것이 발견되었다(Tokida et al., 2007). 정수압, 난류 등 흐름특성과 메탄발생 메커니즘과 연관성을 보여주는 연구도 수행된 바 있다. 메탄 발생 메커니즘은 하상에서 발생한 전단응력과 밀접하다. 하상의 전단응력은 지형 등 복잡한 형태의 함수이다(Joyce and Jewell, 2003). 하상 입자 특성이 세립질로 이루어진 경우는 메탄가스의 기포가 배출되는 형태를 결정하는 중요한 역할을 하기도 한다(Sills et al., 1991; Silva and Brandes, 1998).
하상 외 지리적 요소와 관련성을 보았을 때 호소의 특성도 중요한 관계를 보인다. 호소의 면적은 TP(총인), 용해성 유기물, 수심, 용존산소량과 관련이 있다(Bastviken et al., 2004). 메탄가스 발생은 용존산소량이 적은 무산소 조건에서 유리하기 때문에 호소의 수환경적 특성도 메탄발생에 중요한 요소이다.
메탄발생에는 퇴적물의 특성도 연관성이 있다. 퇴적물에는 각종 유기물 및 미네랄이 포함되어 있어 수생태계와 밀접한 연관성이 있다. 퇴적물은 미생물이 서식할 공간을 제공하기도 한다. 그러나 산업용수 및 생활용수와 같은 오염된 물의 방류량이 증가한다면 유기 오염물질은 증가하게 되며 재차 수생태계 직간접적으로 부정적인 영향을 미친다(Wang et al., 2015). 오염된 퇴적물의 증가는 퇴적층에서의 메탄과 같은 온실 가스의 배출을 증가시킨다(Langenegger et al., 2019). 퇴적물 내에서 메탄 가스 형성은 생산기작이 메탄 산화 및 확산보다 빠를 때 발생하며(Katsman et al., 2013), 이러한 기포는 최종적으로 퇴적물 공극을 빠져나와 수면층으로 용출된다(Dixon et al., 2012). 따라서, 이때 퇴적물의 유기물 함량 및 퇴적물의 입자 크기에 의존한다(Katsnelson et al., 2017). Liu(2019)는 이스라엘의 킨네렛 호의 퇴적물에서 메탄 가스 생성을 측정하였다. 퇴적물 샘플로 용해된 메탄 농도, pH, DOC, 아세테이트 및 황산염을 분석하였다.
이같이 대부분의 연구들은 현장조사를 통해 조건을 정량화 및 일반화하기 어렵다. 따라서, 본 연구에서는 수중 환경 요인에 따른 메탄 생성률을 BMP test를 통해 분석하였다 수중 환경 요인은 생화학 및 수환경적인 요인으로 구성되었으며, 각 요인이 메탄 발생에 미치는 영향은 각 실험 조건에 따른 메탄 잠재량, 최대 메탄 생성율, 및 지연 단계를 통해 분석되었다.
2. 본 론
2.1 메탄 생성 이론
2.1.1 실험적 방법 : BMP test
BMP(Biochemical Methane Potential) test는 혐기성 미생물에 의해 메탄가스로 전환되는 속도와 양을 평가하는 시험이다. Owen et al.(1979)에 의해 개발된 이후로 다양한 분야에서 많은 연구자들에 의해 사용되어 왔다. 일반적으로, 혐기성 분해 반응은 가수분해, 산화발효, 아세트 발효, 메탄발효의 단계로 진행된다. 미세입자는 가수분해에 의해 용해되고 단량체로 전환되며, 단량체는 아세트산 생성 반응을 통해 아세트산, 휘발성 지방산, 에탄올, 이산화탄소 및 수소로 변환된다. 이는 메탄 생성 세균에 의해 아세트산과 수소가 메탄과 이산화탄소로 변환되는 생화학적 반응이다. 분해 과정 중에는 메탄 생성세균과 다른 물질 간의 흡착과 같은 복잡한 물리화학 반응이 발생한다. 이 같은 반응을 실험하기 위해 BMP test는 혐기성 미생물을 포함하는 미생물, 기질, 그리고 영양 배양액 등으로 구성되어 있다. 또한 실험용 용기는 혐기성 조건에서 시간에 따른 메탄 생성을 측정하기 위해 진공상태로 만들어진다.
BMP test의 일반적인 실험 과정은 Fig. 1에 나타난 것처럼 다른 미생물이나 유기물의 영향을 배제하기 위해 수 L에 이르기까지 다양한 크기의 시험용기를 사용하고 해당 용기는 120°C에서 오토클레이브를 통해 살균 처리도 수행한다. 영양 배지, 기질 용액 등의 물질을 주입하고 용기 내 농도는 증류수로 조정할 수 있다. 외부 산소 유입을 방지하기 위해 영양배지는 산소가 포함되지 않은 빌활성 기체인 질소 등으로 퍼징(purging)을 수행한다. 시험물질이 들어있는 시험 용기를 고무마개와 알루미늄 캡으로 밀봉하여 혐기적 조건을 유지하면서 실험을 수행한다.
2.1.2 이론적 방법 : Modified Gompertz model
본 연구에서는 메탄의 양을 이론적 방법에 의해 추정하기 위하여 Modified Gompertz 방정식을 사용하였다. 이 방정식은 일반적으로 미생물 프로세스에서 관찰되는 S-shape 성장 패턴을 설명할 수 있으며, 특히 호수 및 강에서의 메탄 생성 과정을 이론적으로 설명하는 데 자주 사용된다(Fig. 2). 또한, 수생 생태계에서의 메탄 생성 기작을 정량적으로 예측할 수 있는 식을 제공하여 수환경에서의 온실 가스 배출 및 탄소 순환과 관련된 연구가 그간 많이 이루어져 왔다. Modified Gompertz 모형의 방정식은 식 (1)과 같다.
여기서, M은 t시간 후의 메탄 수율(L/kg VS), P는 잠재적 메탄 수율(L/kg VS), R은 최대 메탄 생산율(L/kg VS/day)를 의미한다. λ는 생장지체기를 의미하며 e는 자연상수이다. 식 (1)을 표현하는 그림은 Fig. 2와 같다.
본 연구에서는 각 실험조건에 따른 BMP test 결과로 Modified Gompertz 방정식 형태의 회귀식을 도출하였다. 회귀식을 근거로 각 실험조건에 따른 매개변수를 산정하였다.
2.2 BMP test
2.2.1 실험 재료
실험에 사용된 미생물의 기질은 D(+)-Glucose이다. 셀룰로오스는 Glucose로 된 단순 다당류의 하나로 지구상에서 가장 풍부한 물질이다. 주로 나무와 목화와 같은 식물에서 발견된다. 혐기성 소화에서 Glucose(C6H12O16)의 이론상 최대 메탄 생산량은 표준 조건(1 기압, 0°C)을 기준으로 0.35 L CH4/g COD이다. COD(화학적 산소 요구량)는 호소와 하천의 수질 오염의 대표적인 수질 환경 지표이다. 그러나 혐기성 소화에서 유기 물질이 메탄으로 변환되는 양은 연구 방법이나 유기 물질의 종류에 따라 다양하게 제시되었다. 따라서, 본 연구에서는 유기물질의 양에 따라 메탄발생량을 확인하기 위해 Glucose 용액의 유기물 농도를 수질 측정 기기인 HS 3700 UV/Visible Spectrophotometer를 통해 간접적으로 COD를 측정하였다. 휘발성 고형물은 고체 상태에서 액체 상태를 거치지 않고 즉시 기체 상태로 변환될 수 있는 물질을 말한다. 휘발성 고형물은 일반적으로 물에서의 유기 고형물의 양을 나타내며, 폐수의 정도를 설명하는 데 자주 사용된다. 비연속 배양에서 초기 기질 농도(S0)는 물질대사나 기타 에너지 소비를 위한 탄소 생성 원천으로 작용하며, 초기의 바이오매스 농도(X0)는 기질 반응의 원천으로 볼 수 있다. 낮은 S/X 비율에서는 생장 수율이 높아지는 경향이 있으며, 높은 S/X 비율에서는 반대로 생장수율이 낮아진다. S/X가 0.25~0.5의 범위를 가질 때 산성화의 억제를 최소화하기 위한 적절한 비율로 알려져 있다(Liu, 1996).
본 연구에서는 메탄을 생성하는 메탄생성균으로 국내 2차 하수처리장의 슬러지를 사용하였으며, 이는 대략 휘발성 고형물을 VS 17,000 ± 250 ppm 정도 포함하고 있다. 기질 농도는 수질 오염 정도를 재현하기 위해 COD로 변환하였고, 표준 COD/VS는 산성화의 억제를 위해 0.5로 설정하였다. 또한 퇴적물 특성에 따른 메탄 생성 속도를 분석하기 위해 모래와 점토로 이루어진 퇴적층을 실험 조건으로 설정하였다. 모래(Sand)의 경우 입자가 다른 주문진 표준사와 주문진 규사를 사용하였으며, 점토질 유사는 카올린(Kaolin)을 사용하였다. 주문진 표준사, 주문진 규사, 카올린의 비중은 Table 1과 같이 거의 유사하다. 입경 크기와 점착성 등의 퇴적층 특성을 실험조건으로 설정하였다.
Table 1.
Characteristics of sediments used in BMP test
| Sediments | Mean diameter (m) | Specific gravity | |
| Coarse sand | Jumunjin silica sand | 0.00185 | 2.63 |
| Fine sand | Jumunjin standard sand | 0.0005 | 2.6~2.67 |
| Clay | Kaolin | 0.000003 | 2.6 |
본 실험에서 사용된 영양 배지의 구성은 Table 2에 나와 있으며, 이는 선행연구의 BMP test에서 사용된 영양 배지조건의 범위를 충족시키도록 구성하였다(Kazumi et al., 1997). 조성된 영양 배지는 수질오염이 발생한 하천에서 발생할 수 있는 물질로 구성되어 있으며, 오염물질의 농도는 현장조건보다 높게 구성되었다.
Table 2.
Composition of the test medium
| Nutrient | Stock solution (mg/L) | Test culture (mg/L) |
| KH2PO4 | 5,000 | 500 |
| NH4Cl | 5,300 | 530 |
| CaCl ‧ 2H2O | 750 | 75 |
| MgCl2 ‧ 6H2O | 1,000 | 100 |
| FeCl2 ‧ 4H2O | 200 | 20 |
| NaHCO3 (Buffer) | 20,000 | 2,000 |
2.2.2 실험 조건
본 연구의 실험조건은 온도, 혼합 강도, 퇴적물 특성 및 COD/VS로 구성하였다(Table 3). 먼저, 온도 조건은 28~34°C로 설정하였다. 해당 온도 범위는 호소나 저수지의 하부 층의 평균온도보다는 높지만, 실험기간을 단축시키기 위하여 미생물이 활발하게 활동할 수 있는 온도로 설정하였다. 또한, 기후변화로 인한 수온상승을 감안하였을 때 충분히 가능한 수준의 온도범위라 판단하였다.
Table 3.
Experimental conditions
두 번째, 유기물 및 접종물의 비율에 따른 COD/VS는 0.25, 0.5, 1.0으로 초기에 설정하였다. Case 1의 경우 유기물 및 접종물의 비율의 영향을 확인하고자 수행하였고, 실험결과 가장 최적의 유기물 및 접종물 비율이 0.5로 나타나, Case 2~7까지의 실험은 COD/VS의 조건을 0.5로 설정하였다.
세 번째 조건으로는 수환경의 조건을 나타내는 퇴적물 특성과 혼합 강도이다. 혼합 강도는 RPM으로 전달되는 인큐베이터의 회전을 통해 나타내었다. 일반적으로 실제 호소 및 저수지 내 전단속도는 저수지 크기, 유동 조건 및 지역 특성에 따라 0.01 m/s에서 0.2 m/s의 범위 내로 나타난다(Yazdandoost and Attari, 2004; Garcia, 2008). 본 실험에서는 RPM으로 전단속도 조건을 구분하였고, 실험조건은 90 rpm, 120 rpm, 150 rpm으로 수행하였다. 실험장치 특성상 RPM에 의한 전단속도를 실제로 측정하는데 한계가 있어, FLOW-3D 수치해석에 의해 실험조건과 동일하게 재현하여 각각 0.0203 m/s, 0.0259 m/s, 0.0312 m/s를 도출하였다.
네 번째 조건은 수환경 조건 중 퇴적물 조건인데, 앞서 실험재료에서 언급하였듯이 거친 퇴적층을 나타내는 주문진 규사, 미립토를 나타내는 주문진 표준사, 국내 많은 분포를 보이는 점토질 카올린(H2Al2Si2O8)을 사용하였다.
일반적인 BMP test 과정과 동일하지만 본 연구에서는 수환경을 실험에 적용하기 위하여 시약 용액 주입 후 유기물이 없는 모래가 주입되었으며, 퇴적물에 대한 조건도 함께 적용되었다. Table 3은 전체적인 실험조건을 나타내고 있으며, Fig. 3은 본 실험에서 사용한 반응기의 개념도를 나타낸 것이다.
2.2.3 실험 방법 : 가스측정법
BMP test에서 메탄 생성량은 유기 물질의 휘발성 고형물 당 생성된 메탄 양으로 계산되어 mL CH4/g VS로 표현되지만, 본 연구에서는 COD/VS 조건과 단위를 통일하기 위해 mL CH4로 계산하였다. 본 연구에서는 유리 주사기(10 mL)를 사용하여 48시간마다 생성되는 가스 양을 측정하였다. 피스톤을 반응기 안에서 발생한 가스의 압력만큼 압축하여 압력이 평형 상태에 도달했을 때 체적을 측정하였다. 미생물 소화를 통해 생성된 가스는 메탄이 50~80%, 이산화탄소가 15~45%, 수분이 5%, 그리고 소량의 황화수소(H2S)로 구성되어 있다(McInerney et al., 1979; Seibert et al., 2008). 본 연구에서는 측정된 가스 체적을 표준 상태(STP, 0°C, 1 atm)로 변환하였고, 이 때 사용한 변환식은 식 (2)와 같다.
여기서, 42.2 mmHg는 35°C에서의 포화증기압을 의미하며, 실험 온도 조건에 적합한 포화증기압(28°C에서 28.349 mmHg, 31°C에서 33.695 mmHg, 34°C에서 39.899 mmHg)을 사용하여 산정하였다.
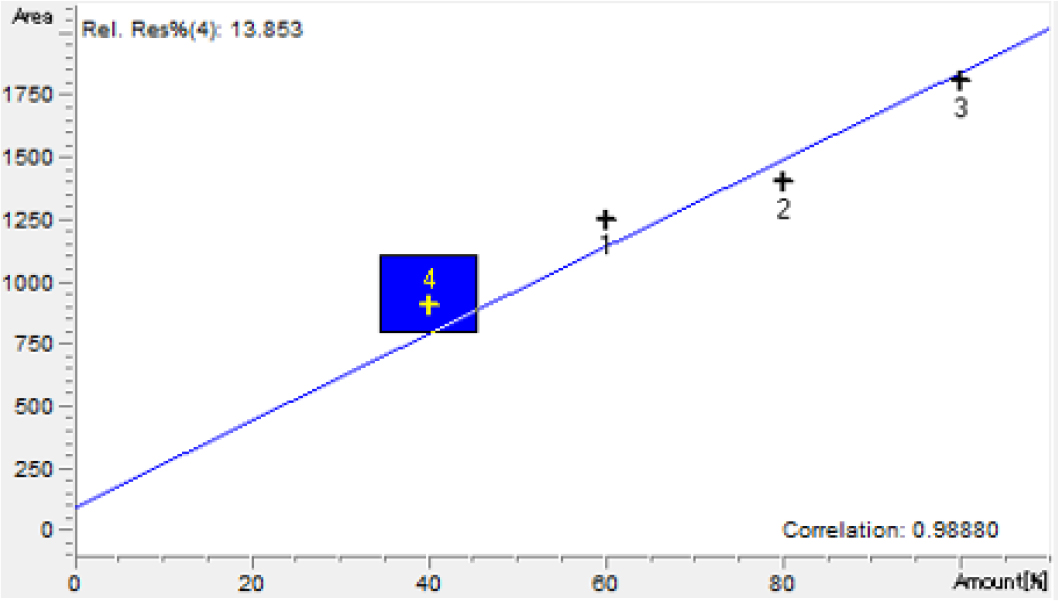
본 연구에서는 생성된 가스 중 메탄에 중점을 두어 측정하였다. 생성된 가스에 함유된 메탄을 측정하기 위해 1 mL의 가스밀봉 주사기를 반응기 뚜껑에 삽입하고 0.2 mL를 측정하여 Gas Chromatography(Agilent 6890 GC)를 사용하여 메탄 비율을 측정하였다. Table 4는 본 실험에서 사용한 GC의 제원과 운영방식을 나타낸 것이다. Table 4에 나타난 것처럼 고순도 질소(99.999%)가 캐리어 가스로 사용되었고, 메탄 가스의 특성을 확인하기 위해 고순도 메탄(99.999%)과 고순도 질소(99.999%)를 혼합한 메탄 표준 가스(100%, 80%, 60%, 40%)도 사용하였다. GC를 활용하여 원하는 가스의 양을 측정하기 위해서는 해당 GC 내 탑재되어있는 표준 가스에 대한 Gas calibration이 필요하다. Calibration 결과, 표준가스와의 상관관계는 0.98로 관측되었다(Fig. 4).
Table 4.
GC operating condition
2.3 실험결과 및 분석
2.3.1 COD/VS 관계 분석
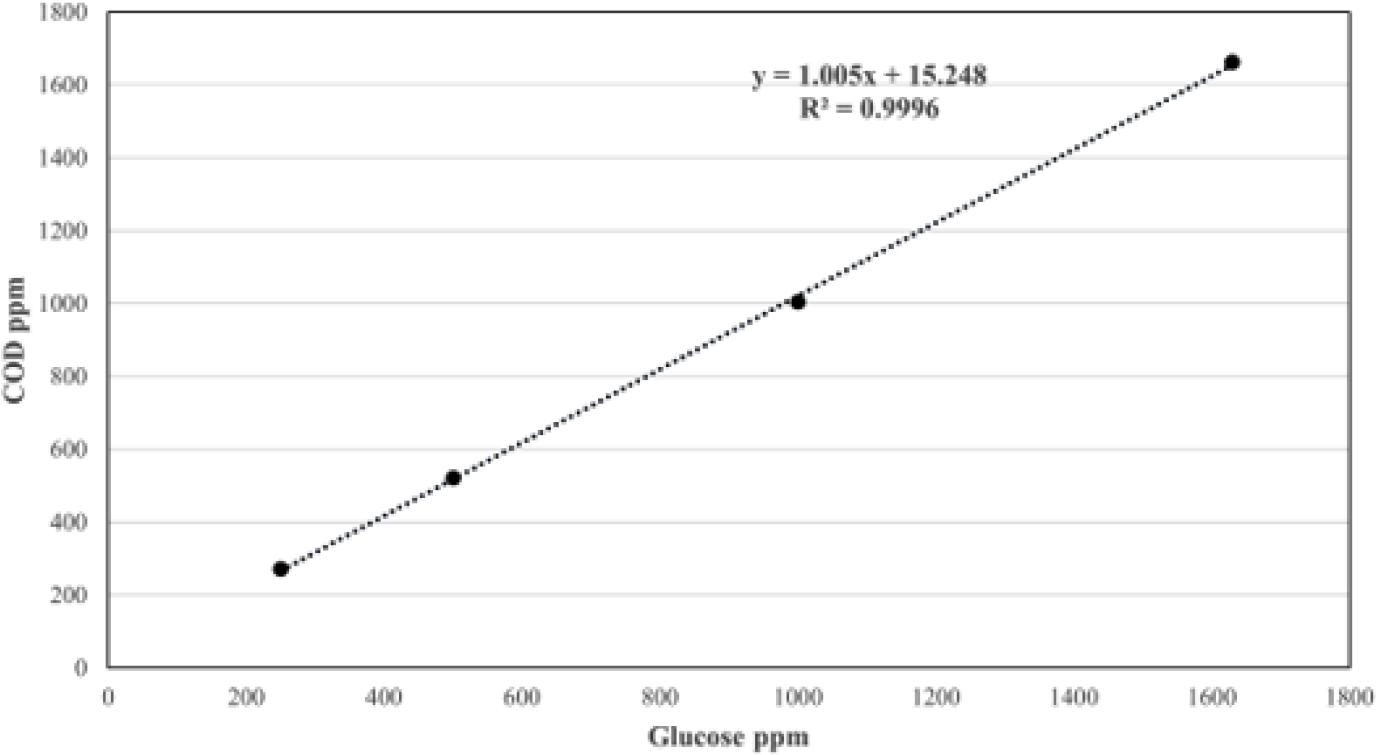
앞서 설명한 것처럼 COD/VS를 측정하기 위해 기기를 활용하였으며, 실험 조건의 용이성을 위해 COD와 Glucose 농도간의 관계를 선행적으로 분석하였다. 그 결과, COD와 Glucose는 선형관계를 나타내었으며, 이론상으로 알려져 있는 관계와 유사함을 확인하였다. Fig. 5에 나타난 것처럼 일차식의 회귀관계를 나타내며, 회귀식에 의하면 300 mg/L의 Glucose을 완전 산화하기 위한 산소요구량은 316.75 mg/L이다. 이론상 산소 요구량인 COD = 320 mg/L과 거의 유사하게 나타남을 확인하였다.
2.3.2 BMP test 결과
실험은 약 300에서 600일 동안 진행되었으며 메탄 수율이 이전 단계 대비 1% 이하로 측정될 때 실험을 종료하였다. 동일한 조건의 실험은 동시에 3개씩 수행되었다. Case 1을 제외하고 COD/VS 조건은 0.5로 설정하였고, 퇴적물 특성에 따른 메탄 생성율을 분석하기 위해 퇴적물이 없는 조건(blank), 점토(Kaolin), 규사(Coarse Sand), 표준사(Fine Sand)로 구성하여 실험을 수행하였다. 수정된 Gompertz 모델을 기반으로 나타낸 메탄 생성률 결과는 메탄 잠재력(P), 최대 생산율(R), 지연 단계(λ)로 Table 5와 Fig. 6에 나타내었다. 모든 실험 결과는 수정된 Gompertz 모델과 상관관계가 0.97 이상임을 확인하였다.
Table 5.
Comparison of historical data and simulation results for power generation
실험 결과, 28°C 및 120 RPM, 31°C 및 90 RPM으로 설정된 Case 2와 Case 5를 제외하고는, Coarse Sand에서 생성된 메탄의 최대값이 가장 높게 나타났으며, Koalin의 경우가 생성 최대값이 가장 낮은 것으로 나타났다. 온도에 따라서는 온도가 증가함에 따라 P, R 및 λ 간의 관계가 명확하게 나타났고, 온도에 따른 생화학적 반응의 가속화로 인해 탄소배출량이 증가하였다. 반면에 흐름특성과 관련된 RPM조건과 관련하여서는 R, λ가 크게 상관관계가 없음을 확인하였다. 본 연구에서는 RPM의 변화가 바닥 전단응력의 변화로 가정하였는데, RPM이 증가함에 따라 물리적인 수리학적 특성요인이 메탄 발생량을 증가시킨다고 판단하였다. 퇴적물 특성과 관련하여서는 큰 입자 크기로 구성된 coarse sand가 P, R에서 가장 큰 증가율을 보인다는 것을 확인하였다. 이는 미생물과의 흡착 표면적이 크며 기공이 상대적으로 충분히 크기 때문에 기포가 순환되기에 충분하다. 반면 점토의 경우 입자 지름이 매우 작기 때문에 응집으로 인한 메탄 분출율이 매우 낮다고 판단하였다.
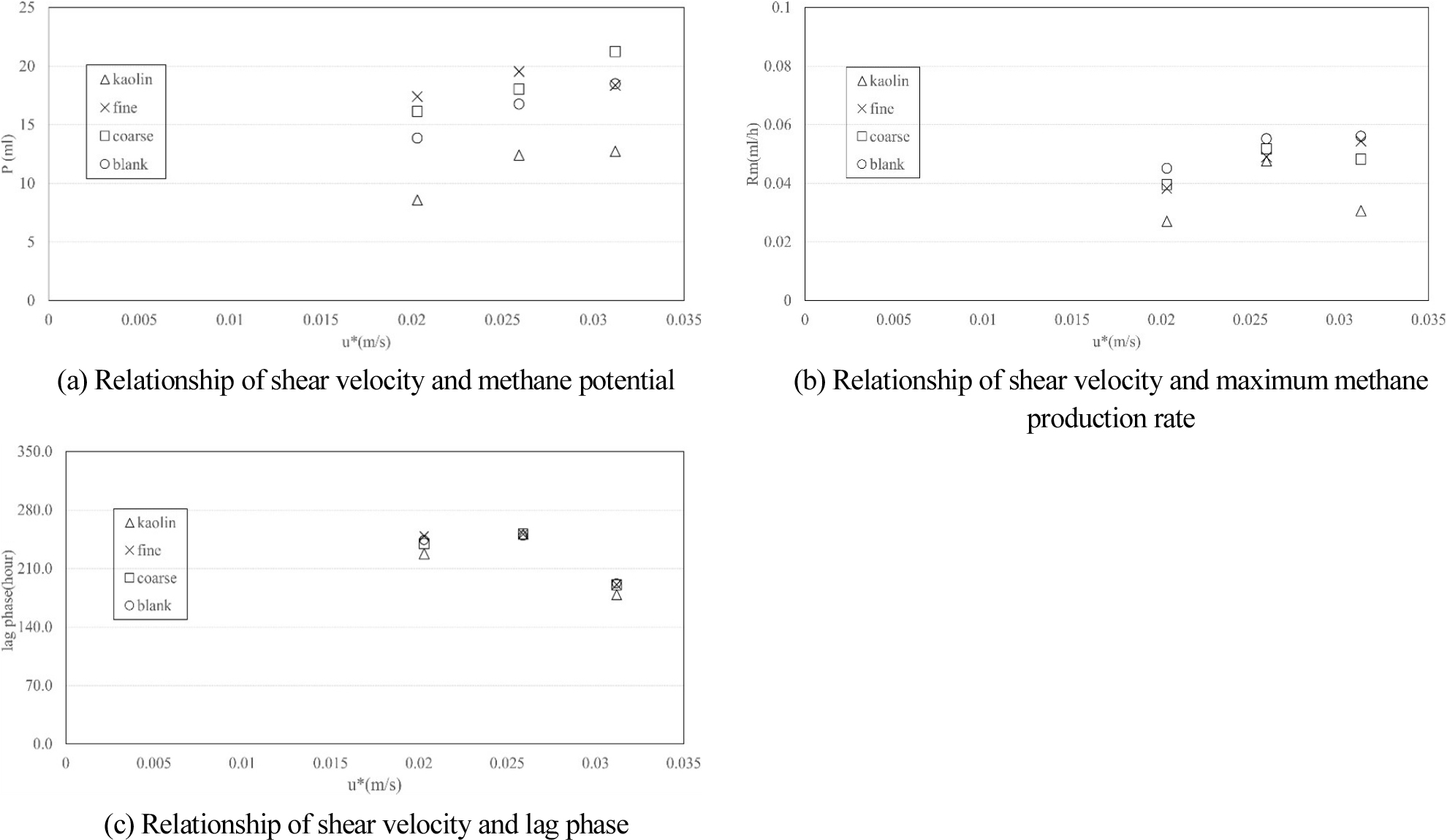
Fig. 7과 Fig. 8은 각각 온도와 메탄 생성률, 전단 속도와 메탄생성률의 관계를 나타낸 것이다. Fig. 7은 온도와 퇴적물의 종류와의 관계를 확인할 수 있는데, 온도가 증가함에 따라 메탄 잠재력과 최대 메탄 생성률은 증가하는 것으로 나타났으나, 지연 시간은 감소하는 것으로 나타났다. 즉, 온도증가에 따라 메탄 발생확률이 높아짐을 의미하는 것이다. Fig. 8의 전단속도의 경우도 온도와 유사한 결과를 나타내었다.
2.3.3 메탄발생량 정량분석
본 연구에서는 메탄 배출량과 물리화학적 요인 간의 관계를 정량화하였다. 총 용해 가스 압력은 식 (3)에 나타난 것과 같이 수직 및 대기 압력에서 수증기 포화 압력을 뺀 것과 같다. 이 때 기포는 퇴적 깊이 아래에서만 형성된다고 가정하였다(Langenegger et al., 2019).
여기서, 는 수심(z)에 따른 메탄의 용해농도(mmol/m3), 는 질소의 용해농도(mmol/m3), 는 메탄의 Henry’s law 휘발성 상수(Pa ‧ m3/mol), 는 질소의 Henry’s law 휘발성 상수(Pa ‧ m3/mol), P에 총 용해 가스압력이며, 는 물의 밀도(1,000 kg/m3), g는 중력가속도(9.81 m/s2), h는 수심(m), 은 대기압(hPa), 는 수증기압이다.
메탄이 발생하여 용출되는 과정은 Henry의 법칙과 관련이 있고, 용해도와 압력과도 연관성이 있다. 그러나 본 연구에서는 압력이 일정한 실험기기 및 반응기를 사용하였기 때문에 압력의 영향을 무시하였다. 퇴적물의 입자 크기와 수체의 전단 유속간의 관계를 분석하기 위하여 무차원 수인 Weber number를 적용하였다.
여기서, ρ은 1,000 kg/m3의 물 밀도, (m/s)은 전단 속도, D(m)는 입자 크기이며 이때, 시약 액체는 하상의 상부에서 반응하기 때문에 하상에 의한 인장력은 무시되었다. 표면장력(σ)은 기포 표면에서의 표면장력 값으로 0.073 kg/sed2로 계산하였다(Levich and Tobias, 1963).
메탄 발생량과 물리화학적 요인 간의 관계는 Fig. 9에 나타난 것처럼 로그함수 분포(y=Cln(x)+K)로 유도되었으며, 웨버 수가 증가하면 메탄 발생량이 증가하는 관계가 도출되었다. K는 온도에 따른 미생물 반응 및 용해도와 관련된 생화학적 요소에 대한 계수이다. 계수 C의 경우 값은 주로 1.2~1.5 정도이지만 이와 관련된 요소와의 상관관계는 확인하기 어렵다. 반면 계수 K는 온도와 관계가 있는 것으로 나타났다.
3. 결 론
메탄의 온실 가스 효과는 같은 양의 이산화탄소(CO2)보다 21배 강력하다. 이러한 메탄 배출 중 하천 및 호소 등과 같은 수체로부터의 발생량이 전체 발생량에 상당한 부분을 차지한다. 혐기성 소화의 산물인 메탄은 특히 오염된 침전 퇴적물로부터메탄 가스 생성 및 용출이 수체에서 발생하는 메탄의 주요 경로로 강조되어 왔다. 수환경으로부터의 메탄 배출에 관한 생지화학 및 환경 요인을 식별하기 위해 다양한 연구가 수행되었지만, 메탄 배출의 추정은 여전히 공간적으로 다양하고 간헐적으로 생성되기 때문에 현실적으로 어려운 실정이다. 따라서, 본 연구에서는 물리화학적 조건인 온도, COD/VS, 전단 속도 및 퇴적물 특성(입자 크기 및 응집 특성) 하에서 메탄 잠재 발생량을 평가하기 위하여 BMP test를 수행하였다. GC를 활용하여 실제 메탄 발생량을 측정하였고, 무차원 수인 웨버함수를 활용하여 메탄발생량과의 관계를 도출하였다. 그 결과, 메탄 생성 속도는 온도와 가장 밀접한 관계가 있음을 확인하였고, 흐름특성인 전단 속도는 메탄 생성보다는 메탄의 용출기작과 연관성이 크다는 것을 확인하였다. 웨버 수는 메탄 용출과의 연관성을 확인하였지만 그 적용 범위가 본 연구에만 한정되어 있기 때문에 모든 현장조건을 일반화하는데는 한계가 있다. 향후 조건범위를 확장하여 일반화할 수 있는 연구방안과 각 주요 변수의 임계점을 정량적으로 도출할 수 있다면 호소 및 하천에서의 메탄발생 및 용출 기작을 정량화할 수 있을 것으로 기대된다.